杏彩体育登录近期,新冠肺炎疫情在印度蔓延。呼吸机、制氧机作为抗击疫情重要的物资在印度需求量较大。2021年4月24日,印度财政部发布第28/2021-Customs公告,取消制氧机(HS 9019/HS 842139)、呼吸机(HS 9019)等18项产品进口关税,至2021年7月31日止。
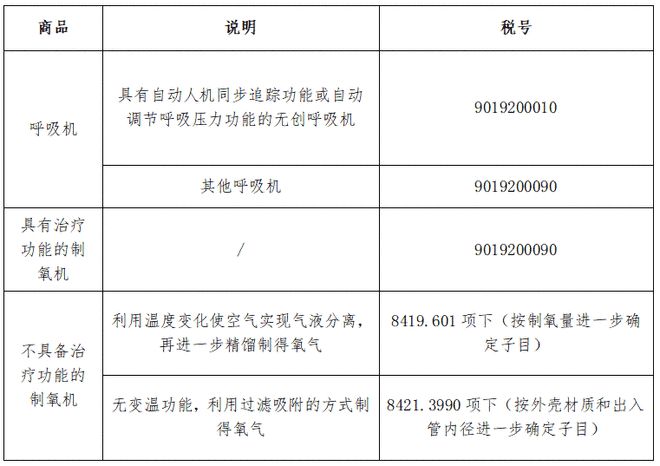
根据《关于有序开展医疗物资出口的公告》(商务部 海关总署 国家药品监督管理局公告2020年第5号)规定,出口呼吸机的企业向海关报关时,须提供书面或电子声明,承诺出口产品已取得我国医疗器械产品注册证书,符合进口国(地区)的质量标准要求,海关凭药品监督管理部门批准的医疗器械产品注册证书验放。
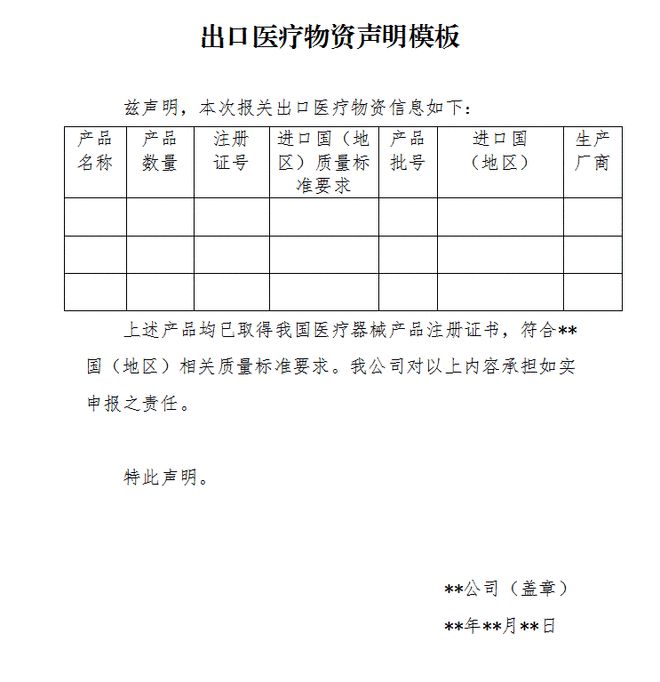
根据《关于进一步加强防疫物资出口质量监管的公告》(商务部 海关总署 国家市场监督管理总局公告2020年第12号)规定,产品取得国外标准认证或注册的呼吸机出口企业,报关时须提交电子或书面声明,承诺产品符合进口国(地区)质量标准和安全要求,海关凭商务部提供的国外标准认证或注册的生产企业清单(清单在中国医药保健品进出口商会网站 动态更新)验放。
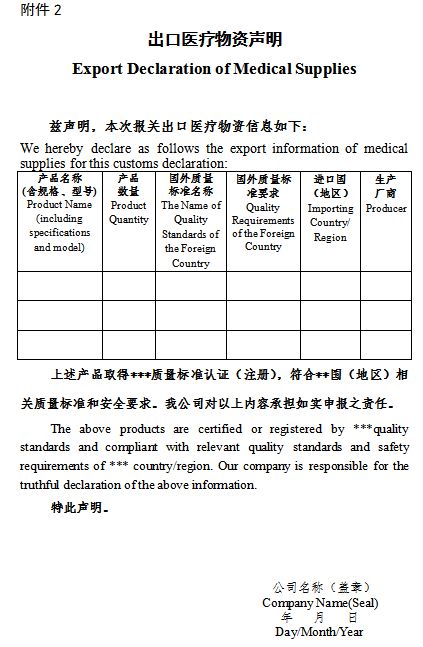
不属于上述公告范围内的呼吸机配件、制氧机等商品,不用按公告要求提供相关单证。但属于医疗器械的,应遵守《医疗器械监督管理条例》(国务院令680号)要求,即:出口医疗器械的企业应当保证其出口的医疗器械符合进口国(地区)的要求。
2017年印度对医疗器械法规进行了大幅修订,公布了《医疗器械管理条例2017》(Medical Device Rules 2017),从2018年1月起实施,参照了“全球医疗器械法规调和会”(The Global Harmonization Task Force,简称GHTF),将医疗器械分为A到D四类,对应从低风险到高风险四种风险级别。
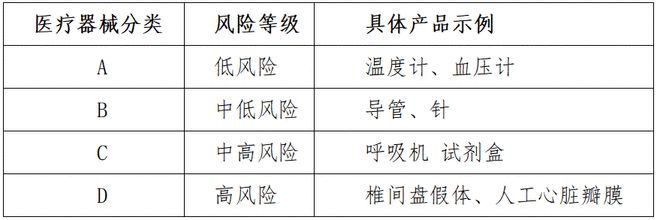
印度CDSCO在2017年也发布了《医疗器械与体外诊疗医疗器械分类标准》,印度要求在申请产品登记时,应遵循印度药品管理总局(DCGI)针对医疗器械的分类决定。对于未能判断分类的情况,应向CDSCO提出分类申请。
出口医疗器械至印度进行销售或使用,必须经印度当地授权代理人(authorised agent)向CDSCO提出医疗器械进口许可证申请(包括A至D级)。CDSCO对医疗器械进口许可证的审核主要分为两步:
首先CDSCO审核授权代理人所提交的生产企业质量管理体系,其必须符合印度医疗器械质量管理标准ICMED 13485(修改采用自ISO 13485,我国标准YY/T 0287等效采用了ISO 13485),包括:生产企业QMS技术文件、检测报告、最近一次现场检查报告等,如果CDSCO认定生产企业QMS的符合存在疑虑时,可以要求实施评估、产品检测或生产企业现场检查(费用由代理人承担)。
如果出口印度的医疗器械分类属于A级或者B级,授权代理人应向CDSCO提交中国的自由销售证明,或者中国实施临床测试的数据(或其他可供证明产品安全性与有效性的数据)。如果出口印度的医疗器械分类属于C级或者D级,授权代理人必须在印度实施临床测试。
例外情况:如果医疗器械(A级至D级)已由欧盟、美国、加拿大、日本或澳大利亚的监管机构颁发了自由销售证明,则无需再进行临床测试。
医疗器械标签要求:该条例第44条规定,应用不可抹掉的墨水在医疗器械的架子包装上或医疗器械的外壳上以及在包装医疗器械的每个外壳上印刷以下内容:
04.关于净数量的正确说明,应以重量、尺寸、体积、单位数量(视情况而定)以及包装中所含设备的数量以公制表示。
12.如果打算将医疗器械作为免费样品分发给医疗专业人员,则在该器械的标签上套印“Physician’s Sample—Not to be sold”字样。
14.如果是进口设备,则在标签上通过粘贴方式提供(如果尚未打印)此类细节,包括:进口许可证编号、进口商的名称和地址、实际生产场所的地址以及制造日期。
15.如果小型医疗器械因为体积原因,无法清晰打印所有信息,则至少应包括产品识别和安全所需的信息。例如:第1、2、3、4条款所涵盖的信息杏彩体育,第5、7、11和13应包括在内。
唯一的器械标识:条例第46条规定,自2022年1月1日起,经批准制造、销售、分销或进口的医疗器械应带有唯一的器械标识,其中应包含器械标识符和生产标识符。其中:
印度财政部已于2021年4月24日发布第28/2021-Customs公告,取消制氧机(HS 9019/HS 842139)、呼吸机(HS 9019)等18项产品进口关税,至2021年7月31日止。印度港口、航运暨水道部也于25日通知各主要港口,取消进口氧气及相关设备的港口处理费,给予优先泊船通关。港务人员必须严格控制船舶入港及货物通关时间,协助物流运作。


